Suche:
- # Berufsbildung
- # Biologie
- # Chemie
- # Deutsch
- # Elementarbereich
- # Englisch
- # Fremdsprache
- # Geografie
- # Geschichte
- # Gesellschaft
- # Gesundheit
- # Grundschule
- # Informatik
- # Kunst
- # Latein
- # Lehrerfortbildung
- # Mathematik
- # Medienbildung
- # Musik
- # Physik
- # Politik / Sozialkunde
- # Religion
- # Sport
- # Technik
- # Umwelt
- # Wirtschaft
Aluminium II
ALUMINIUM II - GEWINNUNG, VERARBEITUNG, RECYCLING Das Metall Aluminium wird auf Grund der besonderen Eigenschaften und der vielfältigen Einsatzmöglichkeiten immer wichtiger.
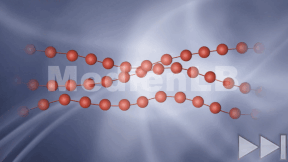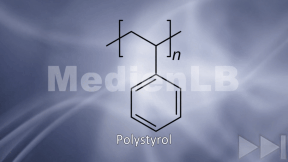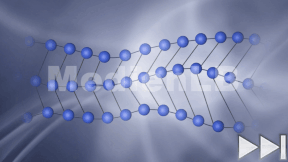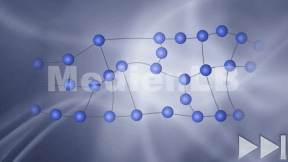
Mehr erfahrenPlastik
Sie basieren auf Kohlenstoffverbindungen, sind preiswert, gut formbar und in den vielfältigsten Erscheinungsformen vorhanden.
Mehr erfahrenAluminium I
ALUMINIUM I - EIGENSCHAFTEN, REAKTIONEN, BESONDERHEITEN Aluminium begegnet uns in der modernen Welt auf Schritt und Tritt. Dies hängt mit den besonderen Eigenschaften des Metalls zusammen. Aluminium ist dabei, Eisen und Stahl aus dem Maschinenbau immer weiter zu verdrängen, da Aluminium einen energiesparenden Leichtbau bei Flugzeugen und Verkehrsmittel aller Art ermöglicht. Aluminium ist widerstandsfähig gegen Witterungseinflüsse, es rostet nicht und eignet sich daher auch als Baumaterial für Häuserfassaden, Fensterrahmen oder einfach für alle Teile, die Wind und Wetter ausgesetzt sind. Dabei hat Aluminium eine edel wirkende Oberfläche, die es als Material für das Wohndesign empfiehlt.
Mehr erfahrenBiogas
Biogas ist eine klimafreundliche regenerative Energiequelle. Es enthält brennbares Methan.
Mehr erfahrenC, CO2 & Co. im Alltag
Alle organischen Stoffe enthalten Kohlenstoff. Im Erdinneren lagert Kohle. Diese entstand vor ca. 300 Millionen Jahren aus Pflanzen in einem Erdzeitalter, das auch als Karbon bezeichnet wird Kohlenstoff bildet bei der Verbrennung organischer Stoffe das Gas Kohlenstoffdioxid. Im Wasser gelöst ist es die sogenannte Kohlensäure, Kohlenstoffdioxid ist ein unbrennbares, farb- und geruchloses Gas, das sich gut in Wasser löst. Mit verschiedenen Metalloxiden oder -hydroxiden bildet es zwei Arten von Salzen: die Carbonate und die Hydrogencarbonate. Es ist in Naturprodukten wie z. B. Kreide und Eierschalen als Calciumcarbonat enthalten. Spezielle Formen, Modifikationen genannt, des Kohlenstoffs sind Graphit und auch der besonders wertvolle Diamant.
Mehr erfahrenLösungen, Emulsionen und Stoffgemische
Im Alltag begegnen uns Stoffe eher selten in ihrer Reinform – viel häufiger haben wir es mit Stoffgemischen zu tun, sei es die Luft, die uns umgibt, die Milch in der Müslischale, der Tee im Glas.
Mehr erfahrenGummi
Heutzutage einen Industriezweig zu finden, der ohne Gummi auskommt, ist denkbar schwierig. In dieser Folge gehen Joey Grit Winkler und Fero Andersen der Frage nach: Was ist Gummi eigentlich und wie wird er hergestellt?
Mehr erfahrenWie Chemiker arbeiten
Chemie begegnet uns permanent im Alltag, beim Kochen, Putzen oder Backen.
Mehr erfahrenKohlenhydrate
Als Kohlenhydrate, auch Saccharide genannt, werden alle Substanzen mit der Summenformel Cn(H2O)n bezeichnet. Kohlenhydrate bilden die Grundlage der Ernährung. In Form von Stärke, Glucose (Traubenzucker), Fructose (Fruchtzucker), Lactose (Milchzucker) und Saccharose (Rüben-, Rohr- oder Haushaltszucker) sind sie uns als Lebensmittel bekannt. Wichtige Kohlenhydrat-Lieferanten sind Kartoffeln und Getreide, wie Reis, Weizen, Mais, Hirse, Roggen und Hafer.
Mehr erfahrenEdelgase
Zu den Edelgasen zählen Xenon, Helium, Neon, Argon, Krypton und das radioaktive Radon. Diese bilden als Elemente der achten Hauptgruppe die Familie der Edelgase. Sie sind allesamt farb- und geruchlos, nicht brennbar und ungiftig. Ihre bemerkenswerteste chemische Eigenschaft ist die Reaktionsträgheit. Diese erklärt sich aus ihrer Elektronenanordnung, die als Edelgaskonfiguration bezeichnet wird und einen besonders stabilen, also energiearmen Zustand darstellt. Zu finden sind die Edelgase in geringen Mengen in unserer Luft, aus der sie auch destilliert werden. Helium wird hauptsächlich aus Erdgas gewonnen. Im Alltag begegnen uns die Edelgase zum Beispiel als Schutz-, Füll- oder Traggase und in Leuchtröhren. Das Schalenmodell beschreibt den Aufbau der Atome. Es geht von einer Verteilung der Elektronen in eingegrenzten Bereichen mit einem festgelegten Abstand rund um den Atomkern aus. Zusammen mit dem umfangreichen Unterrichts- und Begleitmaterial eignet sich die DVD bestens zum Einsatz im Unterricht.
Mehr erfahren